Częstość występowania jaskry (łac. glaucoma, z gr. glaukos, = niebieski) wynosi ok. 1–2%. Jednak wydaje się, że na tę chorobę faktycznie cierpi o wiele więcej osób. W Niemczech z powodu jaskry pod opieką lekarską pozostaje około 700.000 pacjentów. Jaskra to po degeneracji plamki żółtej najczęstsza przyczyna utraty wzroku. Schorzeniu może towarzyszyć normalne lub podwyższone ciśnienie w gałce ocznej. Zgodnie z definicją Europejskiego Towarzystwa Jaskrowego (European Glaucoma Society) mamy tutaj do czynienia z neuropatią nerwu wzrokowego (Nervus Opticus) [11]. Powyższa definicja nie wspomina natomiast o ciśnieniu wewnątrz gałki ocznej.
Z anatomicznego punktu widzenia jaskrze towarzyszy utrata aksonów, komórek glejowych i naczyń krwionośnych oraz zanik nerwu wzrokowego. Jak każda choroba przewlekła, również i jaskra stanowi jeden z objawów schorzenia wielonarządowego. „Chore oczy spotyka się w chorym ciele“ [18]. Dotknięte tym problemem osoby cierpią jednocześnie z powodu migreny, problemów z przesypianiem całej nocy, niskiego ciśnienia krwi oraz zaburzeń rytmu pracy serca. W mózgu takich pacjentów nierzadko stwierdza się defekty widoczne w postaci białych plam (tzw. white matter lesions), które mylnie uznaje się za ślady po mikroudarach. Diagnostycznymi oznakami jaskry są:
- uszkodzenia pola widzenia
- uszkodzenia nerwu wzrokowego
- ewentualnie podwyższenie ciśnienia w gałce ocznej
- zaburzenia przepływu krwi w obrębie naczyń krwionośnych siatkówki
Ograniczenia funkcjonalne przejawiają się początkowo ograniczeniem peryferyjnego pola widzenia, którego chorzy zazwyczaj nie zauważają. Osłabienie wzroku staje się dostrzegalne dopiero w zaawansowanym stadium choroby. Ciśnienie w gałce ocznej wzrasta jedynie u około 60% pacjentów, podczas gdy pozostałych 40% wykazuje prawidłową wartość tego parametru. Uszkodzenia nerwu wzrokowego wynikają z utraty neuronów. Charakterystyczną cechą zanikającej tarczy nerwu wzrokowego jest jego blady kolor. W ramach rozwoju choroby może dojść również do zapadnięcia źrenicy.
Współcześnie przyczyny choroby upatruje się w zaburzeniach ukrwienia, jakimi objęte są wszystkie fragmenty oka. Podczas badań diagnostycznych stwierdza się zarówno absolutne jak i stosunkowe defekty związane z opóźnieniem wypełniania naczyń krwionośnych. Współcześnie za przyczynę tego zjawiska przyjmuje się zaburzenia przepływu krwi w obrębie naczyń krwionośnych, przy czym spadek stopnia ukrwienia dotyczy wszystkich części oka. U pacjentów stwierdza się zakłócenia w wypełnianiu naczyń krwią zarówno w wymiarze absolutnym jak również relatywnym, a także spadek tempa napełniania. Zjawisko to obserwuje się szczególnie w obrębie naczyń, które znajdują się w tylnej części oka. Szczególnie groźna jest fluktuacja poziomu napływu krwi czyli naprzemienne fazy niedokrwienia oraz reperfuzji. Zjawisko to określa się jako pierwotną dysregulację naczyniową (z j. ang. Primary Vascular Dysregulation, PVD) [11]. W fazie niedokrwienia stale uwalnia się NO. Dodatkowo rośnie także poziom czynnika indukowanego hipoksją (HIF1α). Następnie w fazie reperfuzji powstaje ponadtlenek (O °-). Ponadtlenek oraz NO reagują ze sobą tworząc nadtlenoazotyn (ONOO°), który hamuje funkcjonowanie mitochondriów oraz uszkadza aksony.
W przypadku jaskry pierwotnej stwierdzaliśmy następujące zaburzenia metaboliczne:
- zaburzenia mitochondriów [1]
- ograniczenie potencjału antyoksydacyjnego cieczy wodnistej oka [10]
- spadek stężenia witaminy C oraz glutationu [7]
- nasilona peroksydacja lipidów [4] jak również wzrost stężenia dysmutazy ponadtlenkowej [8]. W przypadku wzrostu ciśnienia w gałce ocznej maleje aktywność SOD oraz katalaz i spada stężenie melatoniny, czemu towarzyszy nasilenie peroksydacji lipidów [15].
- nasilona synteza NO w obrębie astrocytów tarczy nerwu wzrokowego [14]
Zaburzenia metaboliczne aktywują astrocyty, które uwalniają następnie cytokiny stanu zapalnego oraz czynniki wzrostu, rozkładając jednocześnie struktury kolagenowe [9].
Źrenica oka cechuje się najwyższym zużyciem glukozy w obrębie nerwu wzrokowego[17]. Rozkład glukozy oraz pirogronianu wymaga obecności kofaktorów enzymu dehydrogenazy pirogronianowej, jakimi są witamina B1 (tiamina) oraz kwas α-liponowy. Co ciekawe, we krwi pacjentów chorych na jaskrę nieodmiennie stwierdza się obniżony poziom witaminy B1 (3).
Zaopatrzenie oka w krew odbywa się dzięki naczyniom krwionośnym siatkówki oraz naczyniówkę (łac. Chorioidea). Tętnica oczna (Arteria ophthalmica) towarzyszy nerwowi wzrokowemu wewnątrz oczodołu, gdzie ulega rozgałęzieniu. Tętnica oczna zaopatruje w krew tarczę nerwu wzrokowego oraz naczyniówkę. Silnie unaczynioną naczyniówkę tworzą tętnice rzęskowe przednie. Ukrwienie tętnic rzęskowych przednich w naczyniówce podlega regulacji przez nerw błędny oraz układ współczulny. Taka wegetatywna regulacja ma również miejsce w tętnicy ocznej, jednak dotyczy to wyłącznie odcinka przed połączeniem się z okiem. Przepływ krwi przez naczynia krwionośne naczyniówki sterowany jest nie tylko przez nerwy błędny oraz układ współczulny, lecz również przez ciśnienie krwi oraz pewne czynniki metaboliczne.
Znaczenie zespołu czaszkowo szyjnego w rozwoju jaskry
Niestabilność stawu szyjnego oraz szyjnego odcinka kręgosłupa to czynniki ryzyka rozwoju jaskry [12], co spowodowane jest przez:
- nawracającą aktywizację układu współczulnego poprzez podrażnianie szyjnej części pnia współczulnego. Klinicznie wyraża się to poprzez wzrost pulsu spoczynkowego, kołatanie serca, wzrost poziomu ciśnienia krwi, czy dodatkowe skurcze serca. Objawy te wywołuje gwałtowne obracanie głową, nagła zmiana kierunku wzroku, pochylanie głowy lub silne odchylanie jej do tyłu. Podwyższona aktywność układu współczulnego w niemieckim systemie opieki zdrowotnej jest klasyfikowana jako osobne schorzenie i oznaczane symbolem M53.0 t (tylni zespół szyjnej części pnia współczulnego). Włókna nerwowe oplatają arterie kręgowe oraz tętnicę A. basilaris niczym pajęcza sieć. Tymczasem skurcz spowodowany reakcją układu współczulnego może ograniczyć ukrwienie mózgu nawet w osiemdziesięciu procentach[6], co wywołuje stan niedokrwienia i z góry skazuje pacjentów na uszkodzenia wywołane repefruzją. Hipoksja indukuje uwalnianie NO, aktywuje HIF1α i może wywoływać stres nitrozacyjny oraz oksydacyjny [9]. Oprócz NO, dostarczanie pirogronianu do cyklu kwasu cytrynowego blokuje również adrenalina, która pobudza działanie kinazy dehydrogenazy pirogronianowej[19]. Jak widzimy adrenalina zagraża przede wszystkim źrenicy, która w warunkach stresu układu współczulnego ulega niewystarczającemu zaopatrzeniu w glukozę.
- Zastój płynu mózgowo-rdzeniowego w pochewce nerwu wzrokowego: Przepływ płynu mózgowo-rdzeniowego między mózgiem a rdzeniem kręgowym jest zsynchronizowany z cyklem pracy serca. Nadmierna ruchliwość stawu szyjnego oraz przemieszczenia dysków szyjnych prowadzą do zwężenia przestrzeni płynu mózgowo-rdzeniowego. Podczas funkcjonalnych badań MRI w postawie pionowej można to udowodnić przy pomocy rotacji, pochylenia lub odchylenia głowy.
Pacjentka R., rok urodzenia 1963
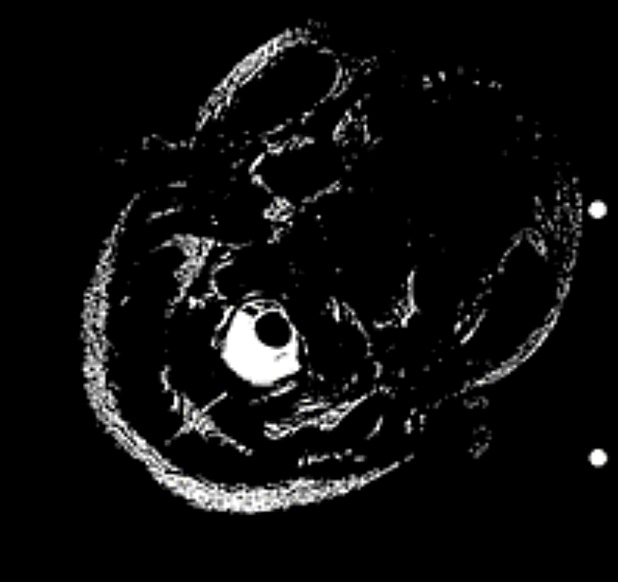
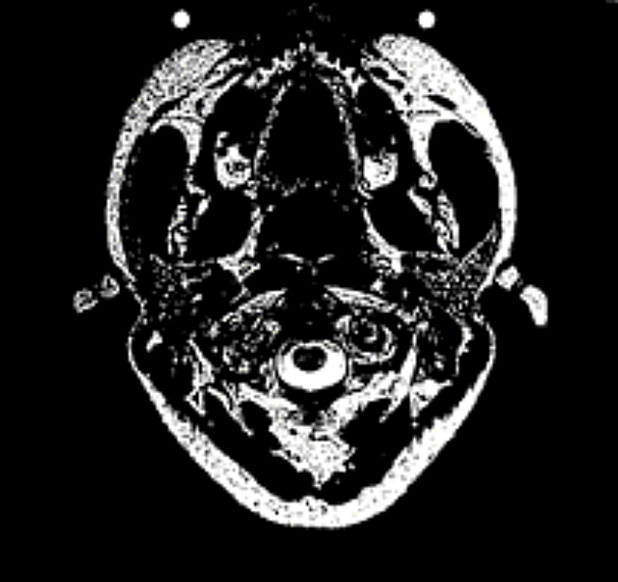
Zdjęcie stawu szyjnego wykonano podczas funkcjonalnych badań MRI w postawie pionowej. Kanał rdzenia kręgowego wykazuje obecność rdzenia kręgowego (ciemny fasolowaty kształt). Otacza go płyn mózgowy (kolor biały) (Rys.1). Charakterystyczne jest to, że już na zdjęciu wykonanym w stanie spoczynku widać zwężenie przestrzeni buforowej na skutek zgrubienia wiązadła poprzecznego (łac. Ligamentum transversum). Przestrzeń buforowa (= odległość pomiędzy szyjnym odcinkiem rdzenia kręgowego a strukturą więzadła) powinna wynosić 4–5 mm. Na zdjęciu widzimy, żejest on zwężony już w stanie spoczynku, czemu towarzyszy ściśnięcie rdzenia kręgowego (który przybrał kształt fasolki).
W normalnych warunkach jest on widoczny jako ciemna, okrągła plama. Podczas rotacji głowy w lewo (Rys.1a) duża część rdzenia kręgowego zostaje podrażniona i wgnieciona. Podczas rotacji głowy (Rys.1b) wyraźnie uwidacznia się zastój płynu mózgowo-rdzeniowego. Zastój ten rozciąga się od szyi aż po pochewkę nerwu wzrokowego.
Rys 1a / Rys 1b
Skutkuje to zaburzeniami przepływu płynu mózgowo-rdzeniowego oraz wzrostem ciśnienia tego płynu w mózgu. W rezultacie spada ukrwienie komórek glejowych oraz neuronów, a poziom enolazy neurospecyficznej NSE oraz białka bariery krew – mózg: S-100 patologicznie rośnie. U osób dotkniętych tym problemem gwałtowne ruchy głową, wstrząsy spowodowane chodzeniem po twardym podłożu, jazda rowerem, motorem czy samochodem, natychmiast podnoszą we krwi poziom NSE i/lub S-100.
Neurony zawierają około 130 peptydów, z których sześć jest neurotoksycznych. Wzrost ciśnienia płynu mózgowo-rdzeniowego prowadzi do jego wyciekania. Wspomniane neurotoksyczne peptydy wydostają się z neuronów do przestrzeni pozakomórkowej. Przykładem takiego białka jest fosforyzowane białko Tau. Tego rodzaju proteiny mogą wywołać uszkodzenia komórek – takie z jakimi mamy do czynienia w przypadku choroby Alzheimera lub – poprzez aktywację limfocytów – doprowadzić do pojawienia się stwardnienia rozsianego [8]. Ogniska glejowe występują w okolicach komory mózgowej oraz pnia mózgowego. W długim okresie opisany mechanizm prowadzi do poszerzenia komory oraz zaniku kory mózgowej.
Niekiedy przy wnikliwej celowej analizie zastój płynu mózgowo-rdzeniowego stwierdza się również w pochewce nerwu wzrokowego. Na skutek kompresji wywołuje on również słabsze ukrwienie nerwu wzrokowego, co pozwala wyjaśnić defekty, które początkowo obserwuje się jedynie w peryferyjnych górnych obszarach pola widzenia, a następnie – koliście – również w dolnych obszarach pola widzenia i w miarę postępu choroby prowadzą do tak zwanego widzenia tunelowego.Zmiany te sugerują uszkodzenia nerwu wzrokowego.
Zator płynu mózgowo-rdzeniowego w pochewce nerwu wzrokowego nie jest widoczny przez cały czas. Zator ten nasilają określone ruchy głową czy pozycja głowy bądź też pionowa pozycja całego ciała [8]. Osoby dotknięte tym problemem odczuwają to poprzez nasilające się bóle głowy oraz zaburzenia widzenia w ciągu dnia. Pozycja leżąca obniża ciśnienie w mózgu, co wyjaśnia dlaczego wyniki badań MRI, które przeprowadzono u leżących pacjentów są nieodmiennieprawidłowe.
Podczas badania MRI mózgu radiolog zauważył u pewnej pacjentki zator płynu mózgowo – rdzeniowego w pochewce nerwu wzrokowego. W konsekwencji kobieta otrzymała więc pilne skierowanie do neurologa w celu obniżenia ciśnienia w mózgu. Tyle, że pacjentka opuściła uniwersytecką klinikę neurologiczną z diagnozą: schorzenie o podłożu psychosomatycznym. Neurologia/psychiatria jako dziedzina nauki nie zna i nie akceptuje do dzisiaj skutków niestabilności stawu szyjnego oraz szyjnego odcinka kręgosłupa. Według lekarzy podczas ostrego ataku w grę wchodziło wyłącznie podawanie Deksametazonu. Jednak przecież nie wolno stosować tego leku przez całe lata. Pacjentom z podobnymi dolegliwościami doradzamy unikanie trzymania głowy w nieprzyjemnych pozycjach oraz wykonywania gwałtownych ruchów a także robienie regularnych przerw i kładzenie się w pozycji horyzontalnej, przy czym ze względów zawodowych w wielu przypadkach często jest to po prostu niemożliwe.
Typowym przykładem niewłaściwej pozycji jest ciągłe pochylenie górnej połowy ciała do przodu z retrofleksją głowy podczas pracy przy laptopie czy komputerze, ponieważ ekran tych urządzeń nie znajduje się na wysokości oczu, głowa pracujących przy nich osób jest bez przerwy pochylona. Osoby dotknięte opisywanym problemem czują po dłuższym czasie spadek ostrości widzenia i zmęczenie oczu. Litery zaczynają się im rozmazywać przed oczami i nie mogą już przeczytać ani linijki więcej. Pojawiają się bóle głowy oraz karku. Noszone ewentualnie okulary przestają pasować.
Procedura
Pacjenci zgłaszają się do naszego gabinetu internistycznego nie z powodu jaskry, lecz przewlekłych chorób wieloukładowych. Podczas wyczerpującej anamnezy okazuje się, że jaskra to jedynie fragment mozaiki, na którą składają się występujące u naszych podopiecznych zaburzenia funkcjonowania wielu różnych narządów. Jeżeli w wywiadzie lekarskim pojawią się przesłanki wskazujące na niestabilność stawu szyjnego, przeprowadzamy następujące badania:
- perymetryczne badania zakresu pola widzenia
- Test Amslera, który pozwala wykluczyć lub potwierdzić degenerację plamki żółtej
- Pulsoksymetria podczas kręcenia głową. Jeżeli w trakcie pulsoksymetrii zostanie stwierdzony wzrost częstotliwości pracy serca lub dodatkowe uderzenia serca, u pacjentów przeprowadzamy dwa badania EKG: w spoczynku oraz podczas obracania głową
- Badanie MRI szyjnego odcinka kręgosłupa w pozycji pionowej oraz badanie otoneurologiczne
- skierowanie do okulisty z prośbą o określenie: pola widzenia w stanie spoczynku oraz po dwudziestosekundowym ciągłym obracaniu głową: czy tego rodzaju aktywność wywołuje lub nasila ubytki pola widzenia. Jeżeli pole widzenia podczas pierwszego badania zostanie ocenione jako prawidłowe, niektórzy okuliści wykonują jeszcze drugie badanie, jednak nie jest już ono konieczne, a warto pamiętać, iż powtórzenie badania nie jest już finansowane przez kasy chorych, a koszty pacjenci muszą ponieść sami.
W 128 przeprowadzonych przez nas badaniach uzyskaliśmy poniższe rezultaty:
brak jakichkolwiek zmian pola widzenia: n = 54
zanik ograniczeń pola widzenia: n = 4*
nasilenie ograniczeń pola widzenia: n = 70
*co sugeruje, że ruchy okrężne głową przywróciły prawidłową pozycję kręgów szyjnych
Dyskusja wyników
Pacjenci cierpiący na jaskrę bardzo często opisują w internecie występujące u nich dolegliwości związane z szyjnym odcinkiem kręgosłupa. Na podstawie wyników uzyskanych w naszym centrum możemy stwierdzić, że związek pomiędzy tymi dwoma zjawiskami jest oczywisty.
Zakłócenia pola widzenia pojawiają się początkowo w zewnętrznych górnych rogach pola widzenia, po czym zaczynają obejmować również dolne regiony. Proces ten opisuje również literatura fachowa. Na istnienie związku między ograniczeniem pola widzenia a niestabilnością stawu szyjnego wskazywaliśmy już w roku 2006 [12], pisząc, że okrężne ruchy głową wywołują lub nasilają tego rodzaju defekty. Niedokrwienie nerwu wzrokowego wywołuje siła nacisku płynu mózgowo – rdzeniowego na pochewkę nerwu wzrokowego.
Poruszanie głową, odchylanie czy pochylanie głowy bądź obracanie głową to ruchy, których w życiu codziennym nie sposób uniknąć. Jednocześnie przez całe miesiące i lata wywołują one niedokrwienie oraz spowodowane następującą po nich reperfuzją, uszkodzenia, które mają swoje konsekwencje. Ponieważ przyczyna niestabilności stawu szyjnego jest nieusuwalna, duże znaczenie mają dla chorych mikroskładniki odżywcze, ponieważ substancje te pozwalają na ochronę neuronów nerwu wzrokowego przed uszkodzeniami.
Nieorganiczna utrata wzroku nieustannie stawia zarówno lekarzy okulistów jak również kardiologów przed dużym problemem. Zazwyczaj lekarze próbują wyjaśnić uwarunkowane działaniem układu współczulnego zaburzenia pracy rytmu serca lub kryzysy związane z wysokim ciśnieniem krwi wyłącznie przy pomocy diagnostyki kardiologicznej. Ponieważ wpływ niestabilności stawu szyjnego najczęściej pozostaje dla oftalmologów oraz kardiologów zagadnieniem zupełnie nieznanym, diagnoza o schorzeniu psychosomatycznym pozostaje jedynie kwestią czasu. Zdarza się to tym częściej, im więcej zdiagnozowanych u pacjenta zaburzeń funkcjonowania niemal wszystkich układów narządów, których przyczyna pozostaje dla lekarza nieznana.
Tego rodzaju pacjenci są wrażliwi na ostre światło, co może prowadzić wręcz do fotofobii. Chorzy noszą okulary przeciwsłoneczne nawet przy normalnym świetle dziennym. Jednocześnie ludzie ci reagują równie wrażliwie na stres, hałas, przeciągi, szybkie zmiany obrazów, zapach chemikaliów oraz etanol.Wszystkie te objawy wskazują na niedostateczne ukrwienie mózgu oraz organów zmysłów. Jednocześnie tam, gdzie odpowiednie przeprowadzane stereotypowe badania nie przynoszą żadnych pewnych rezultatów, na scenę wkracza psychiatria. I tak nadwrażliwość na światło otrzymuje etykietkę „Sunglasses sign“ i zostaje uznane za zaburzenie psychosomatyczne [5]. U jednego z pacjentów postępująca utrata pola widzenia zakończyła się ślepotą, jednak i tutaj diagnoza postawiona przez rzeczoznawcę brzmiała: ślepota psychosomatyczna. Coś niesamowitego.
Opis badania wykonanego u pewnej pacjentki w dniu 3.8.2007: W spoczynku – wyraźne widzenie tunelowe, pole widzenia ulegało jeszcze większemu zawężeniu w wyniku okrężnych ruchów głową. W klinice rehabilitacyjnej po nastawieniu głowy nieoczekiwanie doszło u niej do porażenia nóg oraz wystąpienia ataku epilepsji. W epikryzie widzenie tunelowe określono jako ograniczenie pola widzenia o podłożu psychosomatycznym. (Pacjentka doznała urazu szyjnego odcinka kręgosłupa. Do kliniki rehabilitacyjnej udała się o własnych siłach, a opuściła ją na wózku inwalidzkim z epilepsją oraz znaczną utratą wzroku).
Strategia leczenia
Leczenie samej jaskry pozostawiamy lekarzowi okuliście [18]. Jednak z naszego punktu widzenia nieodzowna jest tutaj również terapia niestabilności stawu szyjnego.
Filary terapii niestabilności stawu szyjnego:
- Wzmocnienie mięśni szyi oraz kręgosłupa
- Unikanie czynników destabilizujących
- Nauka radzenia sobie ze stresem
- Zmiana diety
- Mikroskładniki odżywcze
- Terapia manualna
- ad 1.: najskuteczniejsze są środki, które chorzy mogą podjąć sami. Zaliczamy do nich codzienny energiczny marsz (bez kijków) oraz ćwiczenia izometryczne, służące wzmocnieniu mięśni karku, na przykład przy pomocy specjalnej taśmy Thera-Band.
- ad 2.: Żadnego biegania, jeżdżenia na rowerze, pływania, jazdy konnej, sportów walki, jedynie powolne ruchy głową, unikanie wertykalnych wstrząsów na przykład podczas prac w domu, podczas jazdy samochodem rozgrzewający okład na kark (żadnych kołnierzy ortopedycznych). Żadnego trzeszczenia w szyjnej części kręgosłupa, unikać nadmiernego poruszania głową. Zalecana jest duża ostrożność. Jednak jak ktoś, kto pracuje w zawodach opiekuńczych, jako stomatolog, kasjerka w supermarkecie, czy mechanik samochodowy może poradzić sobie z koniecznością poruszania głową? Należy próbować utrzymywać głowę, szyję oraz klatkę piersiową w jednej linii i unikać maksymalnego przechylania głowy. W nocy należy spać na dopasowanej do indywidualnych potrzeb poduszce oraz unikać spania na brzuchu.
- ad 3.: Przewlekły stres jest trucizną dla układu nerwowego, ponieważ blokuje on dopływ cukru do nerwów, co w szczególności dotyczy znajdującego się w naszej głowie nerwu wzrokowego [13]. Również tutaj najlepiej sprawdzają się te ćwiczenia, które można wykonać w dowolnym czasie i miejscu oraz z łatwością włączyć do programu dnia, na przykład ćwiczenia oddechowe – podczas nich wciągamy powietrze powoli i głęboko. Wszyscy znamy ludowe powiedzenia: „weź głęboki oddech“, „najpierw porządnie odetchnij“. Nerw błędny aktywuje również żucie, na przykład gumy do żucia (bezcukrowej i pozbawionej sorbitolu). Ponadto należy wyrobić w sobie nawyk wieczornej medytacji lub posługiwania się innymi technikami relaksacyjnymi. Działanie antystresowe ma również połączenie magnezu, potasu oraz witaminy C.
- ad 4.: Osoby cierpiące z powodu uszkodzeń szyjnego odcinka kręgosłupa doznają w nocy deficytów energetycznych, na które wskazuje budzenie się w drugiej połowie nocy, pocenie się, koszmary, skurcze mięśni, zgrzytanie zębami a w ciężkich przypadkach – zespół bezdechu sennego. W takiej sytuacji konieczna jest przekąska przed snem czyli spożycie przed snem kromki chleba grubo posmarowanej masłem, a w razie potrzeby – dodatkowa przekąska nocna. W ciągu dnia należy spożywać kilka mniejszych posiłków w ciągu dnia i unikać owoców oraz soków owocowych zawierających duże ilości fruktozy.
| Witamina B12: 500 µg | 1×1 tbl. |
| Kwas foliowy: 400 µg | 1×1 tbl. |
| Biotyna: 2,5 mg | 1×1 tbl. |
| Benfotiamina: 50-300 mg | 1×1 tbl. |
| W przypadku deficytów: | |
| Magnez 300-600 mg w ciągu dnia | |
| Potas 300-500 mg rano | |
| Witamina C 200 mg rano i wieczorem | |
| Kwas alfa-liponowy 200-400 mg |
- ad 5.: przy pomocy mikroskładników odżywczych możemy skutecznie leczyć polineuropatie, jak również uszkodzenia nerwu wzrokowego. Do przydatnych tutaj mikroskładników odżywczych zaliczamy:
- Ubichinol aż do osiągnięcia stężenia we krwi na poziomie 2,5 mg/l
- Lecytynę – dostarczy jej nam spożywanie jajek (3 do 4 jaj w tygodniu, jajka to bogate źródło choliny)
- ad 6.: Terapia manualna: służy przywróceniu właściwej pozycji kręgom szyjnej części kręgosłupa, przy czym nie należy rozluźniać nadmiernie mięśni szyi, ponieważ ich napięcie pełni rolę wzmacniającą oraz amortyzującą. Zachęcamy też do regularnego samodzielnego wykonywania odpowiednich ćwiczeń na co dzień. Rekomendujemy przy tym kierowanie się wskazówkami Ward‘a et al [20], na przykład: kierujemy wzrok w lewo do góry, jednocześnie wysuwając wyprostowany język diagonalnie w prawo w dół i na odwrót. Ćwiczenie to należy powtarzać kilkakrotnie w ciągu dnia (ale nie publicznie!).
U niektórych pacjentów jaskra ustępowała całkowicie nawet mimo wieloletniej historii choroby. Ciśnienie w gałce ocznej normalizowało się, a nerw wzrokowy ulegał regeneracji, co umożliwiało odstawienie leków oraz kropli.
Niektórzy koledzy – lekarze wątpią w autentyczność osiąganych rezultatów. Z naszego punktu widzenia dla powodzenia terapii decydujące znaczenie ma unikanie zastojów płynu rdzeniowo-mózgowego w pochewce nerwu wzrokowego. Skoro po usunięciu na drodze operacji nadmiernego ciśnienia gwałtownie ustępuje chociażby czuciowa polineuropatia obwodowa czy motoryczne parestezje nóg spowodowane uszkodzeniami krążków międzykręgowych lędźwiowego odcinka kręgosłupa, to dlaczego nie miałoby być to możliwe również w przypadku nerwu wzrokowego? Leczenie jaskry będzie skuteczne wówczas, gdy podczas terapii uwzględnimy również występujące schorzenia wieloukładowe.
Studia przypadków pacjentów
Wyniki terapii pacjentki R., U., rok urodzenia 1942
Diagnoza: zespół czaszkowo-szyjny (jazda konna) Terapia: dieta LOGI, witamina B12, kompleks witamin B, witamina B1, lecytyna, koenzym Q10
Badanie kontrolne pacjentki wykonane w dniu 1.8.2008: osłabienie widzenia tunelowego, mimo tego nadal występujące wyraźne ograniczenia pola widzenia, które nasilały się w wyniku okrężnych ruchów głową.
| Przed terapią (lipiec 2007) | Po terapii (czerwiec 2008) |
| zespół bezdechu sennego | ustąpił, aparat CPAP stał się niepotrzebny |
| mrowienie rąk | ustąpiło |
| zespół przewlekłego zmęczenia (CFS) | ustąpił |
| bóle pleców | ustąpiły |
| trudności z oddychaniem przez nos w nocy | ustąpiły |
| zimne stopy | ustąpiły |
| praca w ogrodzie | ponownie możliwa |
| Jednoczesne chodzenie i mówienie | ponownie możliwe |
Ta sama pacjentka podczas badania kontrolnego 3.9.2010: W porównaniu z rokiem 2008 dalsza poprawa pola widzenia, przy czym ograniczenie pola widzenia nadal wywoływały u niej okrężne ruchy głową.
| Dłuższy wysiłek | znowu możliwy |
| Wrażliwość na pogodę | ustąpiła |
| Brak tchu („zadyszka“) przy chodzeniu czy jeżdżeniu na rowerze | ustąpiła |
| Refluks | ustąpił |
| Koncentracja podczas słuchania | bardzo dobra |
| Zaburzenia mowy oraz trudności w doborze słów | ustąpiły |
| Ponadto: ciśnienie krwi – prawidłowe, leki po trzech miesiącach odstawiono Wibracja stawów dużych palców u stóp poprawa z 4/8 na 8/8 Od 9 lat ciśnienie w gałce ocznej rośnie Pacjentka stwierdziła, że „znowu czuje się ogólnie zadowolona“ |
Dziękujemy pani doktor Petrze Fischer oraz panu doktorowi Rainerowi Weuffenowi za współpracę w zakresie badań okulistycznych.
Doz. Dr. sc. med. Bodo Kuklinski
Bibliografia:
[1] Abu-Amera, K. K., Morales, J., Bosley, T. M.: Mitochondrial abnormalities in patients with primary open-angle glaucoma.Invest. Ophthalmol. Vis. Sci. 47 (2006) 2.533–2.541
[2] Aleksidze, A. T., Beradze, I. N., Golovachev, O. G.: Effect of the ascorbic acid of the aqueous humor on the lipid peroxidation process in the eye in primary open-angle glaucoma. Ophthalmol. Zh (1989) 114–116
[3] Asregadoo, E. R.: Blood levels of thiamine and ascorbic acid in chronic open angle glaucoma. Ann. Ophthalom. 11 (1979) 1.095–1.110
[4] Babizhayev, M. A., Bunin, AYa: Lipid peroxidation in open- angle glaucoma. ActaOphthalmol. 67 (1989) 371–377
[5] Bengtzen, R., Woodward, M., Lynn, M. J. et al.:The„sunglasses sign“ predicts nonorganic visual loss in neuro- ophthalmologic practice. Neurol. 70 (2008) 218–221
[6] Betz, E. (Hrsg.): Physiologie und Pathophysiologie der Hirndurchblutung. In: Diethelm, L. (Hrsg.): Handbuch der medizinischen Radiologie. Springer-Verl. Berlin (1981)
[7] Bunin, AIa, Filina, A. A., Erichev, V. P.: A glutathione deficiency in open-angle glaucoma and the approaches to its correction. Vestn. Ophthalmol. 108 (1992) 13–15
[8] Damadian, R. V., Chu, D.: The possible role of cranio-cervical trauma and abnormal CSF hydrodynamics in the genesis of multiple sclerosis. Physiol. Chem. Phys. & Med. NMR 41 (2011) 1–17
[9] Erb, C.: Oxidativer Stress beim primären Offenwinkel- jaskra. Ophtha 5 (2011) 320–326
[10] Ferreira, S. M, , Lerner, S. F., Brunzini, R. et al.: Oxidative stress markers in aqueous humor ofglaucoma patients. Am. J. Ophthalmol. 137 (2004) 62–68
[11] Gerste, A. D.: Glaukom – eine vaskuläre Neuropathie. Dtsch.Ärzteblatt 105 (2008) C489–C490
[12] Kuklinski, B. (Hrsg.): Das HWS-Trauma. Aurum-Verl. Bielefeld (2006)
[13] Kuklinski, B.: Pyruvatdehydrogenase-Kinase – ein Schlüssel-enzym zum Verständnis von CFS, Multiorgankrankheiten und Krebs. OM &Ernährung 150 (2014) F2–F10
[14] Liu, B., Neufeld, B.: Nitric oxcide synthase 2 in human optic
[15] Moreno, M. C., Campanelli, J., Sande P. et al.: Retinal oxidative stress induced by high intraocular pressure. FreeeRadical. Biol. Med. 37 (2004) 803–812
[16] Neubauer, A. S., Kampik, A.: Glaukom – was der Hausarzt wissen sollte. MMV 156 (2014) 44–46
[17] Sperber, G. O., Bill, A.: Blood flow and glucose consumption in the optic nerve, retina and brain-effects of high intraocular pressure. Exp. Eye Res. 41 (1985) 639–653
[18] Strempel, I. (Hrsg.): Glaukom – mehr als ein Augenleiden.Kaden-Verl. Marburg (2013)
[19] Wan, Z., Thrush, A. B., Legare, M. et al.: Epinephrine – mediated regulation of PDK4mRNA in rat adipose tissue.Am. J. Physiol. Cell. Physiol. 299 (2010) C1162–C1170
[20] Ward, R. C., Hruby, R. I., Falls, W. M.: Ingetratives Behandlungskonzept bei Kopf- und Nackenschmerzen.Manuelle Med. 4 (1998) 182–193
[21] Weinreb, R. A., Aung, T., Medeiros, F. A.: The pathophysiology and treatment of glaucoma. JAMA 311 (2014) 1.901–1.911