Starzenie się jest procesem biologicznym uwarunkowanym wieloma czynnikami, który przejawia się zmniejszeniem wydajności czynności fizjologicznych oraz zwiększoną podatnością na wiele chorób, takich jak nowotwory, zaburzenia metabolizmu, cukrzyca, choroby układu sercowo-naczyniowego i choroby neurodegeneracyjne.
Choroby te rozwijają się w wyniku zmian na poziomie komórkowym, takich jak niestabilność genomu, ubytek telomerów, dysbioza, utrata proteostazy, spadek intensywności autofagii, zaburzone rozpoznawanie składników odżywczych, dysfunkcje mitochondriów, starzenie się komórek, zubożenie zasobów komórek macierzystych, zaburzenia komunikacji międzykomórkowej, przewlekłe stany zapalne i zmiany epigenetyczne, które obecnie uznaje się za cechy charakterystyczne starzenia się (Rys. 1).
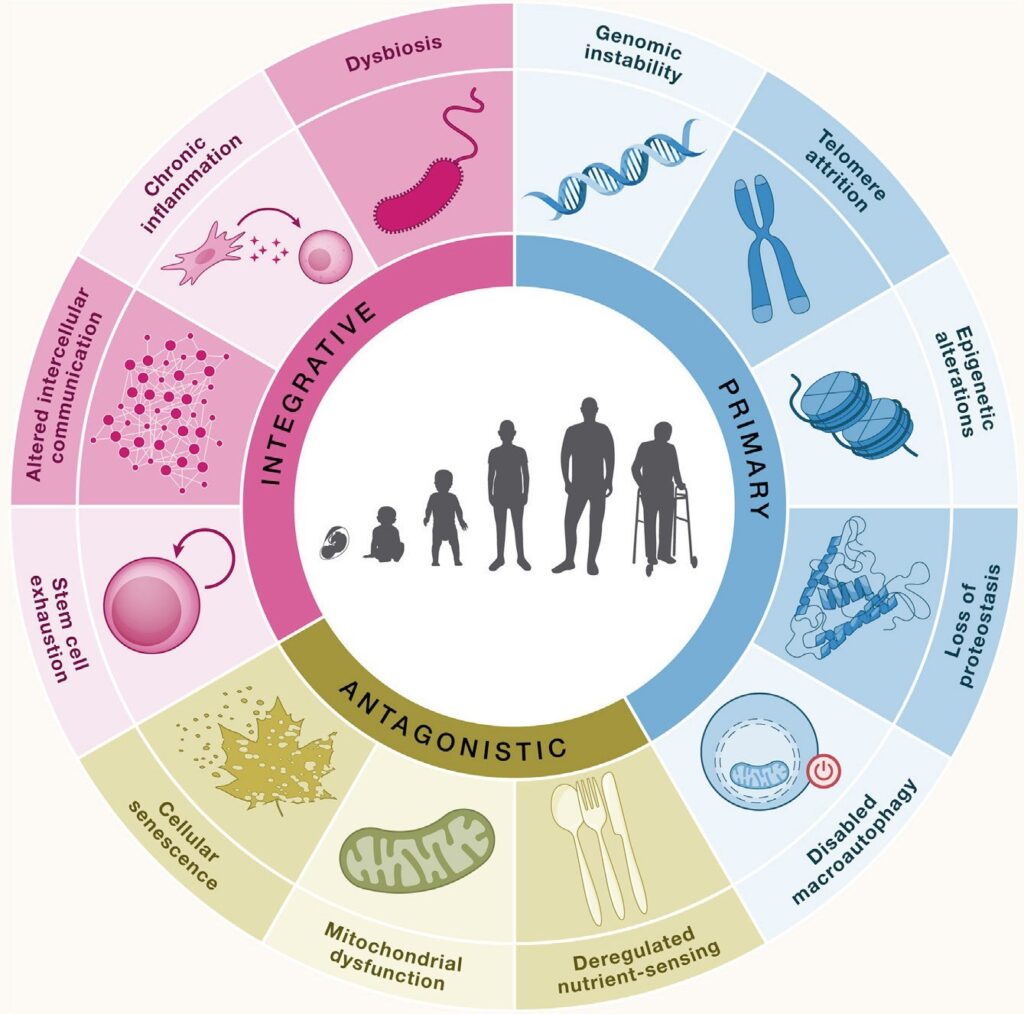
Rys. 1 – Specyficzne cechy starzenia się, na podstawie Lopez-Otin et al. 2023
[opis zgodnie z ruchem wskazówek zegara)
- PIERWOTNE – niestabilność genomu, ubytek telomerów, zmiany epigenetyczne, utrata proteostazy, spadek makroautofagii
- ANTAGONISTYCZNE – zaburzone rozpoznawanie składników odżywczych, dysfunkcje mitochondriów, starzenie się komórek
- INTEGRACYJNE – zubożenie zasobów komórek macierzystych, zaburzenia komunikacji międzykomórkowej, przewlekłe stany zapalne, dysbioza
Według Światowej Organizacji Zdrowia pomiędzy całkowitą długością życia a okresem życia wolnym od chorób pojawia się luka licząca ok. 9 lat. Samo wydłużenie oczekiwanej długości życia zwiększyłoby przedział między okresem życia w zdrowiu a łączną długością życia. Dlatego ważne jest, aby opóźnić rozwój chorób lub ograniczyć ich nasilenie.
Starzenie się i styl życia są ze sobą ściśle powiązane
Możemy w dużym stopniu wpływać na zachowanie zdrowia do późnej starości poprzez wybór optymalnego stylu życia, opartego na zdrowych nawykach, takich jak regularna aktywność fizyczna, zrównoważona dieta śródziemnomorska, wystarczająca ilość snu i celowe suplementowanie substancji, które przeciwdziałają procesom komórkowym odpowiedzialnym za starzenie się. Jednym z najbardziej obiecujących związków mogących dopomóc w zachowaniu na starość zdrowia jest alfa-ketoglutaran (w skrócie AKG).
Czym jest alfa-ketoglutaran?
AKG jest substancją naturalnie syntetyzowaną przez organizm, której stężenie zmniejsza się z wiekiem, i której organizm nie potrafi pozyskać w wystarczających ilościach z pożywienia. AKG jest produktem pośrednim cyklu Krebsa zachodzącego w mitochondriach. Powstaje z izocytrynianu przy udziale dehydrogenazy izocytrynianowej, kluczowego enzymu cyklu cytrynianowego. Następnie ulega przekształceniu w sukcynylo-CoA przy udziale wieloenzymatycznego kompleksu dehydrogenazy alfa-ketoglutaranu, który uwalnia CO₂ i produkuje NADH. AKG jest zatem nieustannie syntetyzowany i rozkładany w cyklu kwasu cytrynowego. Co sprawia, że AKG jest czynnikiem niezbędnym dla przemiany materii i wytwarzania energii w naszych komórkach.
AKG powstaje również w wyniku dezaminacji glutaminianu, który jest aminokwasem wytwarzanym z glutaminy. Reakcje te są odwracalne, dlatego organizm może również syntetyzować glutaminę z AKG (Rys. 2).
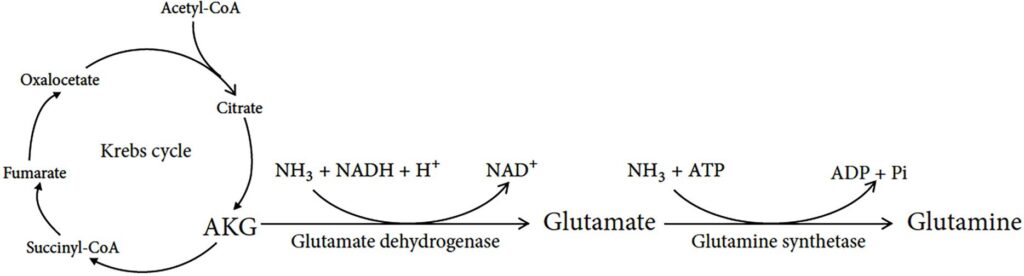
Rys. 2 Jako metabolit cyklu Krebsa, AKG jest niezbędny do przemiany materii i produkcji energii. Źródło: Liu et al. 2018.
Badania dowodzą, że alfa-ketoglutaran wydłuża życie
Rosnąca popularność AKG wynika z jego wpływu na wydłużenie życia oraz szeregu pozytywnych oddziaływań na organizm, które zostały potwierdzone w licznych badaniach.
Pierwszych dowodów na pozytywny wpływ AKG na wydłużenie życia dostarczyły badania na nicieniach z gatunku Caenorhabditis elegans.
Dodanie AKG do pożywki hodowlanej wydłużało żywotność nicieni o 50% i opóźniało pojawienie się fenotypu związanego z wiekiem. U zwierząt traktowanych AKG obserwowano również wzrost autofagii, który prawdopodobnie powodowany był hamowaniem „ssaczego celu rapamycyny” czyli kinazy mTOR.
Potencjał alfa-ketoglutaranu w kontekście wydłużania życia u ludzi udowodniono także w badaniu klinicznym. Analiza metylacji DNA u 42 zdrowych ochotników, którzy przez 7 miesięcy przyjmowali codziennie 1g alfa-glutaranu wzbogaconego wapniem, wykazała znamienne statystycznie obniżenie ich wieku biologicznego o około osiem lat.
AKG znajduje zastosowanie w różnych obszarach zdrowia
AKG dla mocnych kości i mięśni
AKG wspomaga zdrowie tkanki kostnej i mięśni. AKG zapobiega utracie masy i gęstości kości. Takich wyników dostarczyło badanie z podwójnie ślepą próbą, w którym udział wzięło 76 kobiet po menopauzie w wieku 45-65 lat ze zdiagnozowaną osteopenią.
Uczestniczki badania otrzymywały 6g AKG w połączeniu z 1,68g wapnia (Ca-AKG) lub sam wapń w dawce 1,68g. Po sześciu miesiącach w grupie przyjmującej Ca-AKG stwierdzono zmniejszenie poziomu CTX (markera resorpcji kości) o 37% oraz poprawę gęstości kości o 1,6% w porównaniu z grupą przyjmującą wyłącznie wapń.
AKG hamował również spadek syntezy białek mięśniowych i wolnej glutaminy – zapobiegając stanom, które występują zazwyczaj po operacji. Obserwacja ta sugeruje, że AKG nadaje się do leczenia stanów związanych ze wzmożoną degradacją białek, np. po urazach, ciężkich infekcjach, oparzeniach lub zabiegach chirurgicznych. Od dawna jest również popularnym suplementem diety wśród sportowców, ponieważ wspiera syntezę białek w organizmie.
Wspomaganie zdrowej skóry i gojenia się ran
AKG stymuluje syntezę kolagenu i tym samym wspomaga gojenie się urazów i ran, co wykazano u pacjentów z oparzeniami.
Kolagen jest białkiem występującym w naszym organizmie w największych ilościach, lecz po 25 roku życia jego produkcja spada. Kolagen stanowi istotny składnik naszej skóry, zębów, kości i tkanki łącznej. Istotnym kofaktorem enzymów biorących udział w syntezie kolagenu jest witamina C. Wczesna profilaktyka przeciwstarzeniowa z użyciem AKG i witaminy C może zatem opóźniać pojawienie się zmarszczek i pomóc utrzymać dłużej gładką skórę.
AKG odgrywa również kluczową rolę jako przeciwutleniacz, będąc bezpośrednio zaangażowanym w degradację reaktywnych form tlenu (ROS), a także moduluje ekspresję genów kodujących enzymy o działaniu antyoksydacyjnym, takie jak dysmutaza ponadtlenkowa.
AKG a zdrowe jelita
Podawany dojelitowo AKG może służyć bezpośrednio jako źródło energii w błonie śluzowej jelit, bez zwiększania obciążenia azotem. Wskazaniem do podawania AKG mogą być wszystkie przewlekłe choroby jelit, takie jak zespół jelita drażliwego, choroba Leśniowskiego-Crohna oraz wrzodziejące zapalenie jelita grubego. AKG odgrywa również ważną rolę w utrzymaniu bariery jelitowej i regeneracji jelita po urazie lub zapaleniu, np. w przypadku zespołu nieszczelnego jelita.
Wspomaganie mózgu i pamięci
AKG jest wskazany we wszystkich przewlekłych chorobach neurologicznych, takich jak choroba Alzheimera, choroba Parkinsona itp. AKG ulega przekształceniu w glutaminian w procesie aminacji. Dekarboksylacja AKG w obecności witaminy B6 powoduje jego przekształcenie w neuroprzekaźnik GABA o działaniu inhibitorowym. W ten sposób AKG poprawia pamięć długotrwałą i krótkotrwałą. Rys. 3 podsumowuje pozytywne oddziaływania AKG na poszczególne narządy ciała i ogólny stan zdrowia.
AKG jako czynnik ochronny w infekcjach COVID-19 i stanach zapalnych
W badaniu z wykorzystaniem osocza pochodzącego od 103 pacjentów o różnym stopniu nasilenia objawów COVID-19 stwierdzono, że obniżone poziomy AKG mogą stanowić jeden z najważniejszych biomarkerów niekorzystnego przebiegu choroby. Wyniki te sugerują, że ciężki przebieg COVID-19 może być bezpośrednio związany z dysfunkcją mitochondriów. W takim przypadku ograniczenie aktywności cyklu Krebsa i fosforylacji oksydacyjnej powodowałoby zmniejszenie produkcji energii komórkowej w postaci ATP.
W badaniach nad gryzoniami zainfekowanymi COVID-19 podanie AKG zmniejszało akumulację leukocytów, uszkodzenia tkanek płuc w wyniku apoptozy oraz powstawanie skrzepów krwi. Wyniki te sugerują, że podawanie AKG może stanowić strategię zapobiegania zakrzepicy i stanom zapalnym u pacjentów z COVID-19 .
AKG jest dobrze przyswajany przez organizm, szczególnie w postaci soli wapnia (Ca-AKG). Zalecana dawka w celu zapobiegania i spowolnienia procesu starzenia to 1g dziennie. Jednak w przypadku chorób przewlekłych dawka powinna wynosić co najmniej 1,8 g dziennie. AKG uchodzi za związek bezpieczny i dobrze tolerowany; istnieją jednak doniesienia o działaniach niepożądanych ze strony przewodu pokarmowego, takich jak nudności, wzdęcia, wymioty i biegunka, przy dawkach powyżej 10g dziennie.
AKG jest ważnym mediatorem procesów epigenetycznych
Istnieją również liczne nowe dowody na to, że AKG pełni rolę cząsteczki sygnalizacyjnej w kontroli zmian epigenetycznych, takich jak modyfikacje chromatyny i metylacja DNA, które to procesy nasilają się z wiekiem. Epigenetyczna teoria starzenia się jest wynikiem dwóch przeciwstawnych zjawisk. Z jednej strony podstawowy poziom metylacji DNA maleje z wiekiem, zaś z drugiej strony pewne specyficzne zmiany w metylacji DNA nasilają się u osób starszych, niezależnie od płci i rodzaju tkanki. I są przy tym wysoce powtarzalne (Rys. 3).
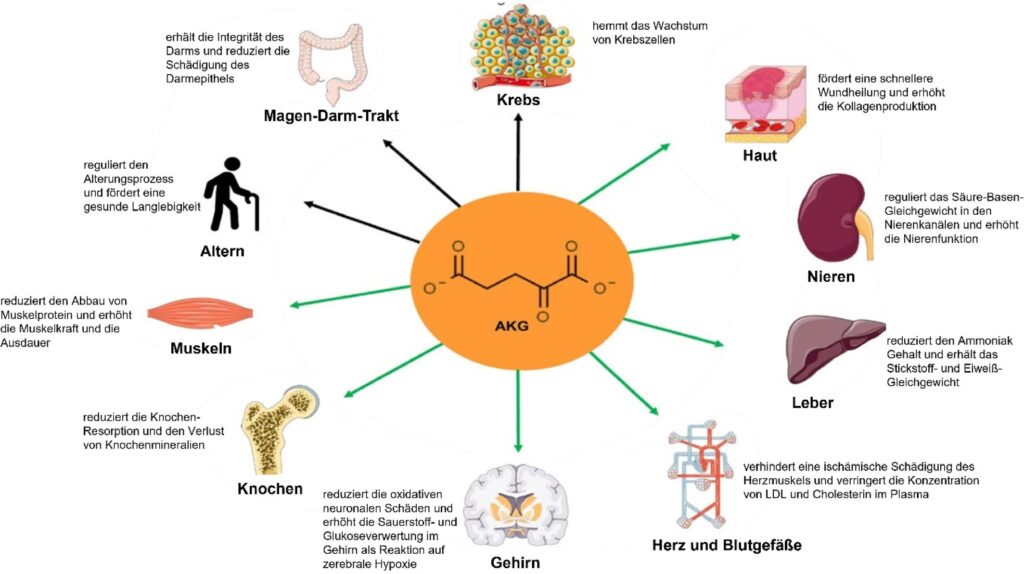
Rys. 3 Wpływ alfa-ketoglutaranu na poszczególne narządy i zdrowie. Zmodyfikowano wg Naeini et al. 2023.
[opis poczynając od KREBS, zgodnie z ruchem wskazówek zegara]
- RAK – hamuje rozrost komórek nowotworowych
- SKÓRA – przyśpiesza gojenie się ran + zwiększa produkcję kolagenu
- NERKI – reguluje równowagę kwasowo-zasadową w kanalikach nerkowych + wspomaga czynność nerek
- WĄTROBA – redukuje zawartość amoniaku + utrzymuje równowagę azotowo-białkową
- SERCE i NACZYNIA KRWIONOŚNE – zapobiega niedokrwiennemu uszkodzeniu mięśnia sercowego + obniża stężenie LDL i cholesterolu w osoczu
- MÓZG – redukuje oksydacyjne uszkodzenia neuronów + zwiększa wykorzystanie tlenu i glukozy w mózgu w reakcji na niedotlenienie
- KOŚCI – ogranicza resorpcję tkanki kostnej + utratę minerałów w kościach
- MIĘŚNIE – ogranicza rozkład protein mięśniowych + zwiększa siłę i wytrzymałość mięśni
- STARZENIE SIĘ – reguluje procesy starzenia + wspiera zdrową długowieczność
- UKŁAD ŻOŁĄDKOWO-JELITOWY – utrzymuje integralność jelit + ogranicza uszkodzenia nabłonka jelitowego
Zjawisko to sugeruje istnienie zaprogramowanej rekonfiguracji epigenetycznej w toku starzenia się, co mogłoby prowadzić do zróżnicowanej ekspresji genów, która z kolei mogłaby wiązać się z występowaniem chorób towarzyszących starzeniu się, takich jak nowotwory. AKG może odwracać takie zmiany epigenetyczne, działając jako kofaktor dla grupy dioksygenaz zależnych od AKG. Do enzymów tych należą „enzymy translokacji dziesięć-jedenaście” (TET1-3), które odpowiadają za demetylację DNA, oraz „enzymy zawierające domenę Jumonji-C” (JMJD), które działają jako demetylazy histonów.
Enzymy „dehydrogenazy izocytrynianowej” (IDH1 i IDH2), które katalizują powstawanie AKG, są często w komórkach nowotworowych zmutowane, co prowadzi do powstawania w miejsce AKG „2-hydroksyglutaranu” (2HG). 2-hydroksyglutaran konkurencyjnie hamuje zależne od AKG dioksygenazy i przyczynia się do rozwoju nowotworu. Dlatego w tkankach nowotworowych często obserwuje się wzrost metylacji DNA (Rys. 4).
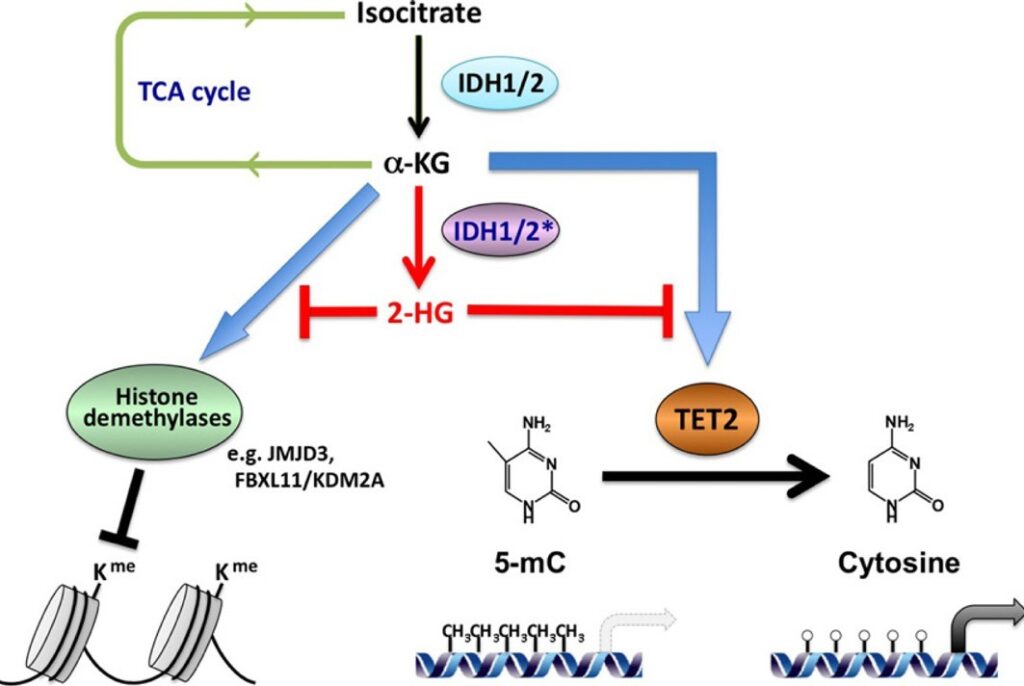
Rys. 4 AKG może odwracać zmiany epigenetyczne związane z wiekiem, działając jako kofaktor dla grupy dioksygenaz zależnych od AKG, które demetylują DNA lub histony.
Kolejna grupa enzymów zależnych od AKG – „hydroksylazy prolilowe” (PHD) – ma istotne znaczenie dla kontroli rozwoju nowotworów. Enzymy te odpowiadają za rozkład czynnika indukowanego hipoksją (HIF1α), jednego z czynników pobudzających rozwój nowotworów.
Hydroksylazy prolilowe (PHD) wymagają obecności AKG, O₂ i jonów Fe2+ jako kofaktorów. W warunkach hipoksji aktywność PHD ulega zahamowaniu pod wpływem niedoboru tlenu, co prowadzi do stabilizacji HIF1α. Dzieje się tak również przy niskich stężeniach AKG. Stabilny HIF1α, który nie jest rozkładany, pobudza ekspresję genów zaangażowanych w angiogenezę, erytropoezę, metabolizm energetyczny, neowaskularyzację, apoptozę i proliferację komórek.
Istnieje również związek między AKG a cukrzycą. Pacjenci cukrzycowi mają niski poziom AKG
Z drugiej strony udowodniono, że AKG zwiększa wydzielanie insuliny w komórkach beta trzustki. Ponadto AKG wykazuje działanie antyglikemiczne poprzez hamowanie glukoneogenezy wątrobowej. Jest to mechanizm, który zachodzi również po podaniu metforminy, jednak AKG ma tę przewagę, że nie wywołuje działań ubocznych. W sercach osób chorych na cukrzycę opisano nieco odmienne markery metylacji DNA.
Suplementacja AKG może przyczynić się do poprawy nieprawidłowych wzorców metylacji DNA poprzez zwiększanie aktywności TET. Mechanizm ten mógłby odwracać uszkodzenia tkanki serca powodowane hiperglikemią poprzez eliminowanie niekorzystnych sygnatur epigenetycznych. Co z kolei mogłoby prowadzić do ograniczenia włóknienia mięśnia sercowego i przywrócenia prawidłowych czynności serca.
Mimo że konwencjonalne terapie normalizują poziom glukozy we krwi, nie są one w stanie powstrzymać rozwoju kardiomiopatii cukrzycowej. Natomiast suplementacja AKG stosowana w trakcie konwencjonalnego leczenia cukrzycy może opóźniać postęp kardiomiopatii.
Podsumowanie
W ciągu ostatnich dwóch dekad medycyna mitochondrialna przeżywa renesans, po części dzięki powszechnej wiedzy, że mitochondria pełnią ważne funkcje biologiczne, które wykraczają poza produkcję energii. W rzeczywistości mitochondria ewoluowały od pasywnych do aktywnych graczy, którzy determinują los i funkcje komórek. Wiadomo, że wraz z wiekiem epigenom – struktura wokół DNA, która kontroluje aktywację i dezaktywację genów – staje się coraz bardziej rozregulowany.
Bibliografia
- B. K. Kennedy et al., „Geroscience: Linking aging to chronic disease,” Cell vol. 159, no. 4, pp. 709–713, 2014, doi: 10.1016/j.cell.2014.10.039.
- C. López-Otín, M. A. Blasco, L. Partridge, M. Serrano iG. Kroemer, „Hallmarks of aging: an expanding universe” [Cechy charakterystyczne starzenia się: rozszerzający się wszechświat], Cell, tom 186, nr 2, s. 243–278, 2023, doi: 10.1016/j.cell.2022.11.001.
- N. Wu, M. Yang, U. Guar, H. Xu, Y. Yao i D. Li, „Alpha-Ketoglutarate: Physiological Functions and Applications” [Alfa-ketoglutaran: funkcje fizjologiczne i zastosowania], Biomolecules & Therapeutics, tom 24, nr 1, s. 1-8, 2016, doi: 10.4062/biomolther.2015.078.
- S. Liu, L. He I K. Yao, „The Antioxidative Function of Alpha-Keto-Glutarate and Its Applications” [Funkcja przeciwutleniająca alfa-ketoglutaranu i jej zastosowania], Biomed Research International, tom 2018, s. 3408467, 2018, doi: 10.1155/2018/3408467.
- R. M. Chin i in., „The metabolite α-ketoglutarate extends lifespan by inhibiting ATP synthase and TOR” [Metabolit α-ketoglutaranu wydłuża życie poprzez hamowanie syntazy ATP i TOR], Nature, tom 510, nr 7505, s. 397–401, 2014, doi: 10.1038/nature13264.
- O. Demidenko i in., „Rejuvenat: potencjalny preparat przedłużający życie zawierający alfa-ketoglutaran i witaminy, zapewnił średnio 8-letnie spowolnienie starzenia biologicznego po średnio 7 miesiącach stosowania, zgodnie z wynikiem testu metylacji DNA TruAge”, Aging, (Albany NY), tom 13, nr 22, s. 24485-24499, 2021, doi: 10.18632/aging.203736.
- R. S. Flip, S. G. Pierzynowski, Perego, B. Lindegard, , J. Wenerman, A. Haratym-Maj i M.Podgurniak, „Alfa-Ketoglutaran obniża poziom C-końcowego telopeptydu, kolagenu typu I (CTX) w surowicy u kobiet po menopauzie z oteopenią: badanie sześciomiesięczne”, Int J Vitam Nutr Res, tom 77, nr 2, s. 89-97, 2007, doi: 10.2024/0300-9831.77.2.89.
- J. Wernerman, R. Hammargvist, E. Vinnars, „Alpha-ketoglutarate and postoperative muscle catabolism” [Alfa-ketoglutaran i katabolizm mięśni pooperacyjny], The Lancet, tom 335, nr 8591, s.701-703, 1990, doi: 10.1016/0140-6736 (90)90881-i.
- L. Cynober i in., “Działanie alfa-ketoglutaranu ornityny, chlorowodorku ornityny i alfa-ketoglutaranu wapnia na poziom aminokwasów i hormonów w osoczu u zdrowych osób”, J Am Coll Nutr, tom 9, nr 1, s. 2-12, 1990, doi: 10.1080/07315724.1990.10720343.
Dr Bodo Kuklinski, “Alfa-ketoglutaran i mitochondria”, OM & Ernahrung. - Rafał Filip i Stefan G. Pierzynowski, „Rola glutaminy i α-ketoglutaranu w metabolizmie jelitowym oraz potencjalne zastosowanie w medycynie i żywieniu.”
- B. Gyanwali i in., „Suplementacja diety alfa-ketoglutarami w celu poprawy zdrowia u ludzi,” Trends in Endocrinology and Metabolism: TEM, tom 33, nr 2, s. 136–146, 2022, doi: 10.1016/j.tem.2021.01.003.
- S. H. Naeini, L. Mavaddativan, Z. R. Kalkhoran, S. Taherkhani i M. Talkhabi, „Alpha-ketoglutarate as a potent regulator for lifespan and healthspan: Evidences and perspectives” [Alfa-ketoglutaran jako silny regulator długości życia i zdrowia: dowody i perspektywy], Experimental Gerontology, tom 175, s. 112154, 2023, doi: 10.1016/j.exger.2023.112154.
- A. Sánchez i in., „Dysfunkcja mitochondrialna, metabolizm lipidów i biosynteza aminokwasów są kluczowymi szlakami w procesie powrotu do zdrowia po covid-19”, Iscience, tom 26, nr 10, s.107948, 2023, doi: 10.1016/j.isci.20231.107948.
- M. N. Schrimali i in., „α-Ketoglutarate inhibits thrombosis and inflammation by Prolyl Hydroxylase-2 Mediated inactivation of Phospo-Akt” [Alfa-ketoglutaran hamuje zakrzepicę I stan zapalny poprzez inaktywację fosfo-Akt za pośrednictwem prolyl hydroxylase-2], EBioMedicine, tom 73, s. 103672, 2021, doi: 10.1016/j.ebiom.2021.103672.
- O. Gangisetty, M. A. Carbera, I S. Murugan, , „Impact of epigenetics in aging and age related neurodegenerative diseases”[Wpływ epigenetyki na starzenie się I choroby neurodegeneracyjne związane z wiekiem], Front Biosci, (Landmark Ed), tom 23, nr 8, s. 1445-1464, 2018, doi: 10.2741/4654.
- H. Nakajima i H. Kumioto, „TET2 jako aktywny regulator epigenetyczny prawidłowej I nowotworowej hematopoezy”, Cancer science, tom 105, nr 9, s.1093-1099, 2014, doi: 10.1111/cas.12484.
M. Hoang i J.W. Joseph, “Rola alfa-ketoglutaranu i szlaku wykrywania niedotlenienia w regulacji funkcji komórek trzuski”, Islets, tom 12, nr 5, s.108-119, 2020, doi: 10.1080/19382014.2020.1802183.